DIABETES NEWS No.185
|
 | |||||||
2型糖尿病に対する薬物療法アルゴリズム
-日本糖尿病学会コンセンサスステートメント-
-日本糖尿病学会コンセンサスステートメント-
東京女子医科大学 内科学講座 / 糖尿病・代謝内科学分野 教授・基幹分野長
馬場園哲也
馬場園哲也
このたび日本糖尿病学会のコンセンサスステートメントとして、2型糖尿病の薬物療法のアルゴリズムが発表されましたので紹介します(糖尿病65:419-434, 2022)。
◆アルゴリズム作成に至った経緯
血糖降下薬選択に関するわが国独自の提言を行う理由として、日本人と.欧米人における、2型糖尿病の病態、エビデンスに基づいた治療戦略、さらには血糖降下薬の処方実態の差があげられています。具体的には日本人では欧米人に比べて肥満者の割合が少なくインスリン分泌低下の関与が大きいこと、動脈硬化性血管障害の発症率が少ないこと、ビグアナイド薬の処方が少なくDPP-4阻害薬が多く処方されていること、などです。特にビグアナイド薬として最も多く処方されているメトホルミンのエビデンスは、実は限定的であることが知られています(Diabetes News No.178「メトホルミンを再度,再評価する」)。◆血糖降下薬選択の4つのステップ
このアルゴリズムは4つのステップ、すなわちStep1は病態に応じた薬剤選択として肥満合併の有無Step2は安全性への配慮、Step3はadditional benefits (付加的な利点)、さらにStep4は考慮すべき患者背景からなっています。Step1で、本文中には肥満症例における候補としてビグアナイド薬、SGLT2阻害薬、チアゾリジン薬、 GLP-1受容体作動薬およびイメグリミンが良い適応と記載されていますが、アルゴリズムではDPP-4阻害薬とα-グルコシダーゼ.阻害薬が併記され、グリニド薬とスルホニル尿素薬が除かれています。
Step2「安全性への配慮」では、低血糖リスクが高い症例、腎機能障害例、心不全合併例において避けるべき薬剤が記載されています。
Step3「Additional benefitsを考慮すべき併存疾患」として、最近のエビデンスに基づき慢性腎臓病、特に顕性腎症、心不全、さらには心血管疾患におけるSGLT2阻害薬とGLP-1受容体作動薬の有用性が示され最後のStep4「考慮すべき患者背景」として、服薬遵守率と医療費があげられています。詳細は原著をご参照ください。
◆今後の課題
日本人におけるエビデンスが少ないなか、本アルゴリズムは、日本糖尿病学会コンセンサスステートント策定に関する委員会が中心となって、熱心に議論されたものです。特に優先する血糖降下薬を設けなかったこれまでのわが国の方針から、薬剤の選択の際考慮すべき4つの点を明示した点で、実地医科の先生方にとっても有意義なアルゴリズムであろうと思います。今後わが国のエビデンスの蓄積により必要な改定が行われ、糖尿病診療の向上に繋がることを期待したいと思います。
|
|
基礎インスリン注入量を自動制御する
ハイブリッドクローズドループシステム
ハイブリッドクローズドループシステム
東京女子医科大学 内科学講座 /
糖尿病・代謝内科学分野 助教
髙木 聡
糖尿病・代謝内科学分野 助教
髙木 聡
◆インスリンポンプとSAP
インスリンポンプは皮下にカニューレを留置し、体外からインスリンを持続注入する機器です。2014年12月にインスリンポンプ単体ではなく、連続皮下ブドウ糖濃度測定(continuous glucose monitoring:CGM)を同期させて稼働させるSAP(sensor-augmented pump)という機器が使用可能となりました。このポンプには高血糖や低血糖時にアラートを出す機能が付帯しています。私たちは最近、頻回注射法やインスリンポンプ単体使用の1型糖尿病患者さんがSAPを開始することで、HbA1cが低下し治療満足度が向上することを明らかにしました(Diabetol Int 13:280-287, 2022)。
2018年3月には、CGMで低グルコースを検出した場合や、近いうちに低グルコースになることが予想される場合インスリン注入を自動的に停止し、低血糖を回避するpredictive low-glucose management(PLGM)という機能が付いたインスリンポンプの使用が開始されました。
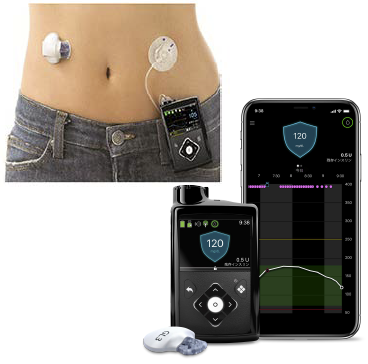
◆HCLの概要
今回ご紹介するHCLは前述のPLGMをさらに発展させたものと言えます。PLGMは低グルコースを予測してインスリン注入を自動停止していましたが、高グルコース時にインスリンを増量する機能はありませんでした。HCLは、低グルコース時にインスリンを減量もしくは一時停止、高グルコース時はインスリンを増量するといったベーサルインスリン量の調整をポンプが自動で行い、120mg/dLに設定された目標血糖値に近づけるように調節します(この機能をオートモードと言います)。ただし、食事の際のボーラスインスリン量の自動調整はできず、ポンプに血糖値や食事の炭水化物(糖質)摂取量などを入力して決定する必要があります。これがハイブリッドと言われる所以で、まだ完全なクローズドループシステムを達成するには至っていません。海外ではいくつかのHCL製品が使用されていますが、国内で使用可能なのは日本メドトロニック株式会社製ミニメド770Gシステム®です(図)。
◆HLCの効果と注意点
HCLの導入による血糖コントロールの改善や治療満足度の向上が報告されています(Diabet Med 39:14863,2022,Diabetes.Res Clin Pract 177:108876, 2021)。一方で、HCLを使用するうえで注意しなければならない点がいくつかあります。まず、オートモードは高血糖が長時間持続する場合などいくつかの状況で停止し、マニュアルモードに戻ることがあります。また、食前のボーラスインスリンはオートモードボーラスという機能を使用しなければなりません。この機能を使用する場合は、カーボカウントが必要となります。ほかに、指先穿刺による血糖測定が1日数回以上必要であること、医療費が頻回注射法より高額になること、さらにインスリンポンプ全般に共通する点として、カニューレの抜けなどによるインスリン注入不足で高血糖になる恐れがあることなどにも留意する必要があります。
インスリン治療中で血糖コントロールに難渋している患者さんの中で、インスリンポンプ療法に興味を持たれている方には、HCLの導入を検討する価値があると思います。
|
|
動脈硬化疾患予防ガイドラインが改訂されました
東京女子医科大学 内科学講座 /
糖尿病・代謝内科学分野 助教
長谷川 夕希子
糖尿病・代謝内科学分野 助教
長谷川 夕希子
東京女子医科大学 内科学講座 /
糖尿病・代謝内科学分野 教授
中神 朋子
糖尿病・代謝内科学分野 教授
中神 朋子
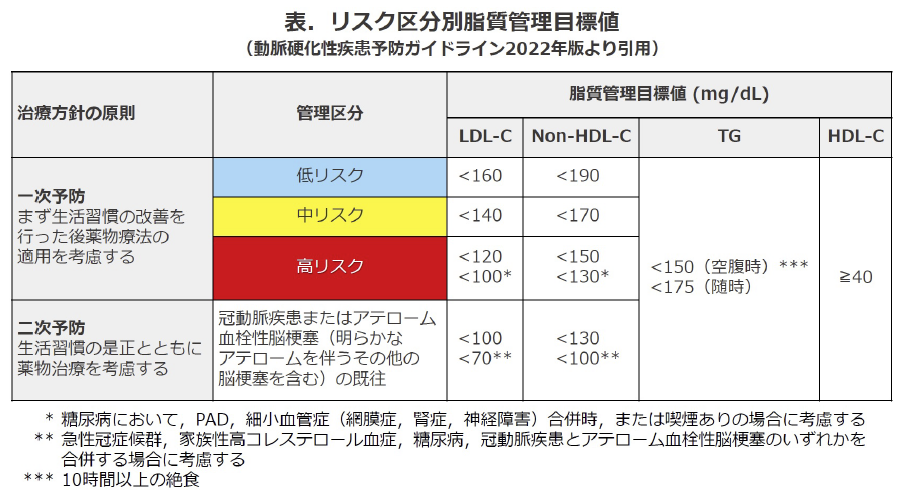
◆随時トリグリセリド(TG)値の採用
これまで内外のガイドラインでは、血清TGを空腹時採血でのみ評価し、150mg/dL以上を高TG血症としていました。今回の改訂では、随時採血で175mg/dL以上でも高TG血症と定義することになりました。すでにヨーロッパのガイドラインでは、随時TG175mg/dL以上も高TG血症としています。◆動脈硬化性疾患の絶対リスク評価
2017年版ガイドラインで採用された吹田スコアは、冠動脈疾患をアウトカムとする絶対リスクを推計していました。2022年版では、動脈硬化性疾患の絶対リスク評価の手法に冠動脈疾患とアテローム血栓性脳梗塞の2つをアウトカムとする久山町研究のスコアリングテーブルが採用されました。◆糖尿病患者の脂質管理目標値(表)
冠動脈疾患の既往のない日本人2型糖尿病患者5,042人を対象としたEMPATHY試験では、平均37か月の追跡で強化療法群(平均LDL-C 76.5mg/dL)、通常療法群(104.1mg/dL)を比較した結果、強化療法群で脳イベントが48%減少しました。この結果を基に、心血管イベントリスクを有する日本人2型糖尿病患者の一次予防にでは、LDL-C 100mg/dL未満を目標とされました。◆動脈硬化性疾患の二次予防(表)
冠動脈疾患またはアテローム血栓性脳梗塞の二次予防では、糖尿病などの高リスク患者におけるLDL-C目標値を一律70mg/dL未満とされました。今回の改訂では,糖尿病患者のより厳格な脂質管理が提唱されています。なお糖尿病患者の管理目標値を一律とするのではなく、リスクの程度に応じた血清脂質管理とする必要があるといえるでしょう。